Почти 100% бактериальных инфекций теперь можно выявить менее чем за 3 часа
Ученые сделали важный прорыв в точности и скорости, с которой можно выявлять и лечить часто смертельные инфекции, вызванные патогенами. Время, которое зачастую критически важно для спасения жизни пациента.
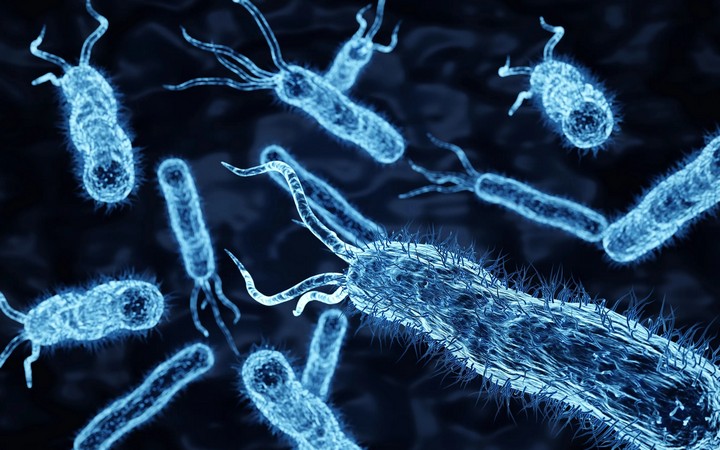
Новая методика диагностики
Учёные из Национального института науки и технологий Ульсана (UNIST) в Южной Корее представили свою новую диагностическую методику, известную как флуоресцентная гибридизация in situ (FISH), использующую искусственные полимеры – пептидную нуклеиновую кислоту (PNA), которая служит зондами для связывания с различными генетическими последовательностями в бактериях. Когда две молекулы зондов связываются с целью, излучаются флуоресцентные сигналы, которые фактически показывают отпечаток разных патогенов.
Как работает метод FISH
"Техника флуоресцентной гибридизации in situ (FISH) позволяет быстро обнаружить и идентифицировать микробы, основываясь на их вариациях в геномной последовательности, без необходимости в трудоемком культивировании или секвенировании", отмечают ученые. "Однако недавний взрыв данных о микробных геномах сделал сложной задачу разработки подходящего набора зондов для микробных смесей. Мы разработали новый набор PNA-основанных зондов FISH с оптимальной специфичностью к целям, проанализировав вариации последовательности рибосомной РНК 16S у всех видов бактерий."
Статья по теме на LifeGlobe.net: Могут ли бактерии разрушать пластик?
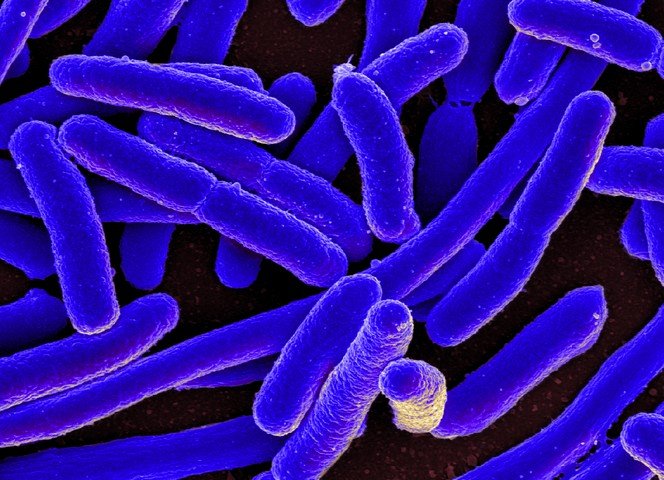
Результаты работы метода FISH
В лаборатории метод FISH выявил семь видов бактерий, которые часто инфицируют людей: Klebsiella pneumoniae, Proteus mirabilis, Bacillus subtilis, Enterococcus faecalis, Escherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus. Он показал точность более 99% для всех видов, кроме S. aureus – патогена, который инфицирует кожные ткани, для которого точность была всё равно высокой, 96,3%. Некоторые выявления достигли 99,9%.
Как достигается высокая точность
"Обнаружение основано на передаче энергии Фёрстера (FRET) между парами соседних связывающихся зондов PNA, что исключает взаимные помехи между видами", сообщили ученые. "Быстрая последовательная идентификация видов была реализована с использованием химически разделяемых флуорофоров, без ущерба для точности обнаружения. Благодаря высокой точности и улучшенной скорости этот набор методик имеет большой потенциал для клинического применения."
Разработка технологии
Хотя может показаться, что метод достаточно прост, эффективность системы скрывает огромную работу, проведенную для её разработки. Команда проанализировала 19 885 известных генетических последовательностей 14 614 видов бактерий, а затем разработала видоспецифические последовательности PNA для нацеливания на рибосомную РНК бактерий. Зонды PNA имеют явные преимущества перед традиционными ДНК-зондами и могут проникать через клеточные стенки патогенов. Присоединение двух зондов к одному и тому же патогену повышает точность, особенно в случаях, когда болезнь вызвана несколькими патогенами.
Преимущества метода
Кроме того, метод FISH может дать результаты менее чем за три часа. Традиционные диагностические инструменты, такие как анализы крови и полимеразная цепная реакция (ПЦР), могут занять от нескольких дней до недель. Для пациентов, борющихся с инфекциями, которые угрожают жизни, такими как сепсис, крайне важно диагностировать и лечить как можно быстрее.
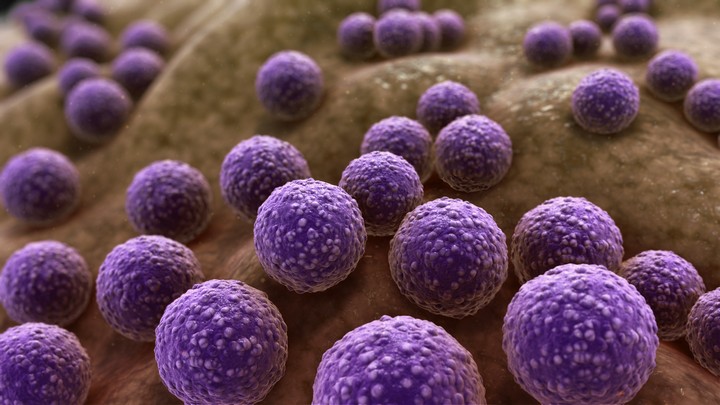
Потенциал метода для медицины
Быстрая обработка результатов также помогает избежать назначения пациентам неправильных антибиотиков.
"Этот метод поможет в диагностике инфекций, требующих немедленного лечения антибиотиками, таких как сепсис, инфекции мочевых путей и пневмония, а также поможет сократить ненужное использование антибиотиков", сказал главный автор исследования доктор Сунхо Ким из Отдела биомедицинской инженерии UNIST.
Дальнейшие шаги
Теперь команда проведет дополнительные испытания на образцах крови, взятых от больных пациентов, чтобы оценить, насколько хорошо метод FISH работает в клинических условиях.
Читайте далее: Забытые изобретатели эпохи Позолоченного века
Редакция LifeGlobe.netПросмотров: 530
 Инфракрасные сигналы могут раскрыть жизнь на "водных мирах"
Инфракрасные сигналы могут раскрыть жизнь на "водных мирах" Солнечные часы Сарагосы
Солнечные часы Сарагосы Остатки нефти могут использоваться в недорогом углеродном волокне
Остатки нефти могут использоваться в недорогом углеродном волокне Испытательная башня ТиссенКрупп
Испытательная башня ТиссенКрупп Загадочные руины Дехистана: исчезнувший город в пустыне Туркменистана
Загадочные руины Дехистана: исчезнувший город в пустыне Туркменистана Новое крупнейшее офисное здание в мире превзошло Пентагон
Новое крупнейшее офисное здание в мире превзошло Пентагон ИИ научился выявлять рак эндометрия с точностью 99%
ИИ научился выявлять рак эндометрия с точностью 99% Японская компания изобрела «стиральную машину» для людей
Японская компания изобрела «стиральную машину» для людей Аэропорт Царицы Тамары: Футуризм в горах Грузии
Аэропорт Царицы Тамары: Футуризм в горах Грузии Гуманоидные роботы на сборочном конвейере: создание копий самих себя
Гуманоидные роботы на сборочном конвейере: создание копий самих себя