Грибок из гробницы Тутанхамона может лечить рак
Некоторые учёные предполагали, что спящие споры обнаруженного в гробнице Тутанхамона грибка стали причиной гибели нескольких археологов, принимавших участие в раскопках. Однако теперь этот грибок получил новое значение — как источник перспективных противоопухолевых соединений.

От проклятия фараона — к терапии лейкоза
Исследователи из Университета Пенсильвании (UPenn) обнаружили, что грибок Aspergillus flavus, ранее обвиняемый в таинственных смертях археологов, содержит уникальные молекулы с мощными свойствами против рака. После выделения и модификации этих соединений учёные добились значительного эффекта в борьбе с лейкозом — формой рака крови.
«Грибы подарили нам пенициллин», — говорит профессор Шерри Гао, соавтор исследования и специалист в области химической и биомолекулярной инженерии. — «Наши результаты показывают, что в природе всё ещё скрыто множество ценных лекарственных соединений».
Особенности грибка A. flavus
Aspergillus flavus входит в крупный род грибов, насчитывающий около 250 видов. Он распространён по всему миру и встречается в почве, сене, зёрнах и разлагающейся растительности. При длительном воздействии может вызывать аллергию, астму, синусит и более серьёзные заболевания дыхательной системы. Однако миф о его смертельных спорах до сих пор вызывает споры в научной среде.

Цель учёных — не история, а будущее
Исследователи сосредоточились не на прошлом грибка, а на его потенциале. Из A. flavus были выделены специфические соединения, относящиеся к группе рибосомно-синтезированных и посттрансляционно модифицированных пептидов (RiPPs). После структурной доработки они показали способность эффективно подавлять деление раковых клеток. Их активность сопоставима с действием препаратов, одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
RiPPs синтезируются в рибосомах — ключевых органеллах клетки, отвечающих за производство белков. По сути, рибосома — это «повар» клетки, который по рецепту (мРНК) собирает аминокислоты и «готовит» необходимые белки для жизнедеятельности организма.
Сложность синтеза — источник силы
«Синтез этих соединений довольно сложен», — отмечает Цюйюэ Ни, первый автор исследования и постдокторант UPenn. — «Но именно это делает их такими биологически активными».
Статья по теме на LifeGlobe.net: Могут ли микробы и бактерии жить в космосе?
Новые соединения: асперигимицины
Команда исследователей выделила четыре разных RiPP-соединения, получивших название асперигимицины. Два из них показали особенно сильное воздействие на раковые клетки. Учёные также выявили, что один из генов — SLC46A3 — способствует активному проникновению этих соединений внутрь клеток.
«Этот ген действует как ворота», — объясняет Ни. — «Он не только помогает асперигимицинам проникать в клетки, но может быть полезен и для доставки других циклических пептидов».
Как асперигимицины блокируют рак
Дополнительные исследования показали, что асперигимицины нарушают деление раковых клеток. «Клетки рака делятся бесконтрольно», — объясняет Гао. — «Асперигимицины блокируют образование микротрубочек, необходимых для этого процесса».
Интересно, что воздействие асперигимицинов ограничивалось клетками лейкоза и не оказывало аналогичного эффекта на клетки рака груди, печени или лёгких. Это делает соединение высоко специфичным и перспективным в качестве будущего направленного лечения.
В то время как тысячи RiPP-соединений уже найдены у бактерий, у грибов они являются редкостью. Именно это делает открытие асперигимицинов особенно важным. «Хотя обнаружено всего несколько грибковых RiPPs, почти все из них обладают выраженной биологической активностью», — подчёркивает Ни. — «Это неизведанная область с огромным потенциалом».

Следующий шаг — испытания на животных
В дальнейшем команда планирует провести испытания асперигимицинов на животных моделях. В случае успеха возможно проведение клинических исследований на людях, хотя до этого ещё предстоит пройти долгий путь.
«Природа — это невероятная аптека», — заключает Гао. — «Наша задача — раскрывать её секреты. Как инженеры, мы рады учиться у природы и использовать эти знания для создания новых решений».
Редакция LifeGlobe.netПросмотров: 320
 Почему Марс стал мёртвой планетой: виновато Солнце
Почему Марс стал мёртвой планетой: виновато Солнце Город будущего от знаменитых архитекторов поднимется из песков Аравии
Город будущего от знаменитых архитекторов поднимется из песков Аравии Как кофе связан со здоровым старением: данные 30-летнего исследования
Как кофе связан со здоровым старением: данные 30-летнего исследования Может ли популярный подсластитель повысить риск инсульта?
Может ли популярный подсластитель повысить риск инсульта?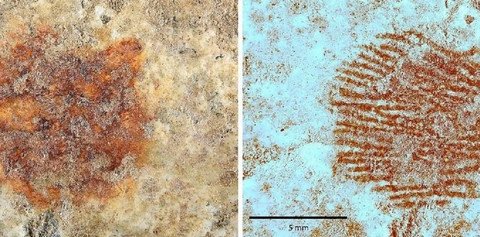 Археологи обнаружили 43-тысячелетний отпечаток пальца неандертальца
Археологи обнаружили 43-тысячелетний отпечаток пальца неандертальца Египетский синий: Воссоздание пигмента возрастом 5000 лет
Египетский синий: Воссоздание пигмента возрастом 5000 лет Голиаф: самая большая лягушка на грани исчезновения
Голиаф: самая большая лягушка на грани исчезновения Сверхзвуковые полеты возвращаются после полувекового запрета
Сверхзвуковые полеты возвращаются после полувекового запрета Почему бабуины передвигаются цепочкой: это человеческая черта
Почему бабуины передвигаются цепочкой: это человеческая черта Гигантские залежи золота находятся под нашими ногами — и они недоступны
Гигантские залежи золота находятся под нашими ногами — и они недоступны